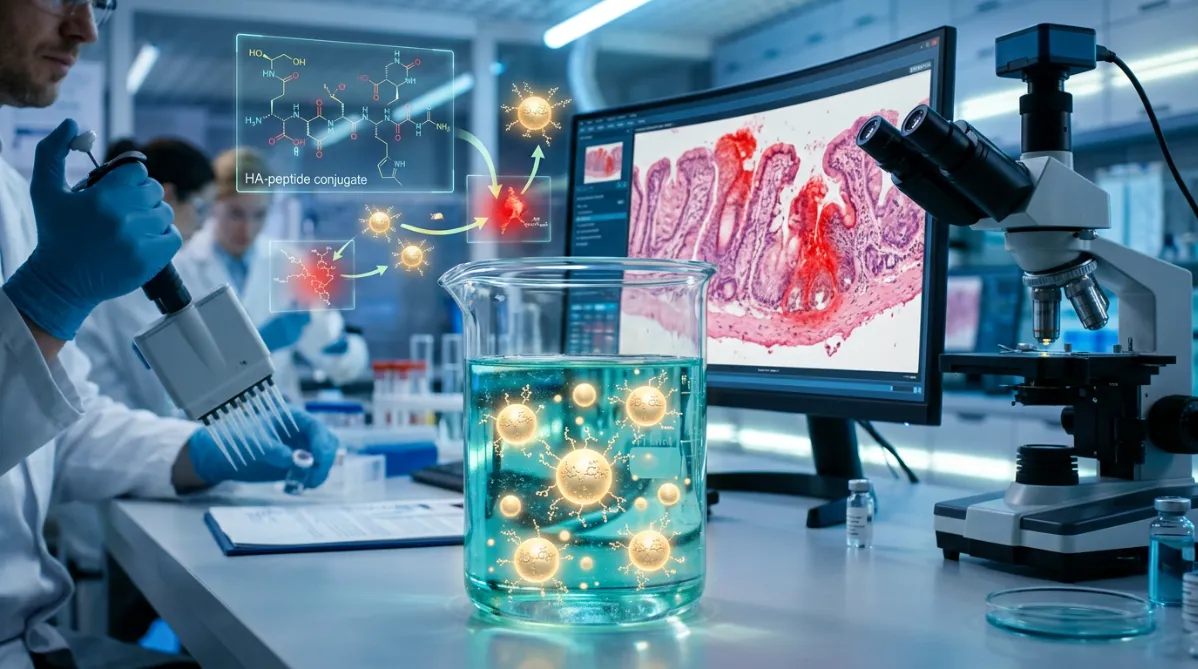
靶向肽递送的突破性进展
已有全新药物递送系统问世,有望彻底改变溃疡性结肠炎等炎症性肠病的治疗。乔治亚州立大学和西南大学的研究团队成功研发出透明质酸功能化的纳米颗粒,能够精准将治疗性肽递送至炎症肠组织,为全球数百万患者带来新希望。
该创新系统解决了现代医学中最顽固的难题之一:在体内准确递送治疗分子至靶部位,并将副作用降至最低。传统口服药物常因吸收不良、在消化系统中快速分解以及全身非特异性分布导致疗效下降并出现不良反应。
KPV 三肽:大自然的抗炎因子
这项突破的核心是赖氨酸‑脯氨酸‑缬氨酸(KPV),它是一种来源于激素 α‑黑色素细胞刺激素(α‑MSH)的天然三肽。虽分子小,但抗炎活性显著,是治疗炎症性肠病的理想候选分子。
“KPV 代表了肽类治疗的重大进步,”未参与本研究的胃肠病学专家 Sarah Mitchell 博士解释道。“与常伴显著副作用的合成药物不同,这种天然来源的化合物能够配合机体自身的抗炎通路。”
KPV 通过调节关键的炎症信号通路——包括在炎症反应中起核心作用的核因子‑κB(NF‑κB)通路——发挥抗炎作用。当肠道发生炎症(如溃疡性结肠炎)时,KPV 能帮助恢复促炎与抗炎信号之间的微妙平衡。
然而,KPV 的治疗潜力长期受到口服后稳定性差、降解迅速的限制。肽类分子在胃酸和各种消化酶的作用下极易被分解,导致难以通过胃肠道实现有效递送。
透明质酸:完美的载体
研究团队的解决方案是将 KPV 包裹在功能化透明质酸(HA)纳米颗粒中。透明质酸是一种遍布人体的天然高分子,在本递送系统中发挥多重关键作用:
靶向识别
透明质酸可特异性结合 CD44 受体,而 CD44 在炎症肠上皮细胞及参与炎症性肠病的免疫细胞表面高度表达。受体介导的靶向确保药物负载精准送达病灶部位。
提升稳定性
HA 包衣能够保护封装的 KPV 免受胃酸和消化酶的降解,使更多活性分子完整到达目标组织。
增强生物利用度
相较于自由肽的给药方式,纳米颗粒配方显著提升了 KPV 的吸收和利用率,进而在炎症部位达到更高的治疗浓度。
黏附特性
透明质酸具备黏膜粘附性,可与肠道黏液层紧密结合。此黏附作用延长了纳米颗粒在肠道的停留时间,实现持续释放。
纳米颗粒工程:分子层面的精确控制
打造高效的纳米递送系统需要在分子层面进行精准的工程设计。研究团队对以下关键参数进行了细致优化:
粒径与分布
纳米颗粒直径约为 100‑200 nm,这一尺寸范围兼具以下优势:
- 足够小,可穿透黏液屏障;
- 足够大,避免被肾脏快速清除;
- 适合通过内吞作用被细胞摄取。
表面电荷
表面电荷影响颗粒与生物膜的相互作用以及在体液中的稳定性。HA 功能化提供了适中的负电荷,既促进细胞摄取,又保持颗粒的悬浮稳定。
药物装载效率
研究人员实现了高装载率,确保每个纳米颗粒携带足量的 KPV,帮助降低总剂量,从而减少潜在副作用。
释放动力学
颗粒设计为在较长时间内持续释放 KPV,保持目标部位的治疗浓度,同时将系统性暴露降至最低。
对溃疡性结肠炎治疗的临床意义
在美国,溃疡性结肠炎约影响 100 万人,导致大肠慢性炎症,常见症状包括血性腹泻、腹痛和急迫性排便。当前的治疗手段主要包括:
传统疗法
- 5‑氨基水杨酸(5‑ASAs):常作为一线抗炎药,但并非对所有患者均有效。
- 皮质类固醇:抗炎效果显著,却伴随长期副作用。
- 免疫抑制剂:抑制免疫系统,但增加感染风险。
- 生物制剂:靶向治疗,费用高且可能随时间失效。
现有方案的局限
- 非特异性分布导致系统性副作用;
- 患者间疗效差异大;
- 随时间产生耐药或失效;
- 生物制剂成本高,需频繁给药或采用侵入性给药方式。
新递送系统的优势
透明质酸功能化纳米颗粒系统能够缓解上述诸多问题:
- 靶向递送:通过 CD44 受体专门定位于炎症组织,降低健康组织的药物暴露。
- 提升疗效:更高的生物利用度和靶向性使炎症部位药物浓度升高。
- 降低给药频次:持续释放特性有望实现更少的给药次数,提高患者依从性。
- 成本效益:使用天然 KPV 与 HA 有望相较于昂贵的生物制剂降低整体治疗费用。
- 安全性提升:天然来源的药物及载体提示良好的安全特性。
实验验证与结果
研究团队开展了系统的临床前研究,以评估递送系统的有效性。关键发现包括:
体外实验
- 证实纳米颗粒能够特异性结合炎症细胞表面的 CD44 受体;
- 观察到 KPV 在 24‑48 小时内持续释放;
- 在细胞培养模型中展示出显著的抗炎活性。
动物实验
- 小鼠溃疡性结肠炎模型显示结肠炎症显著减轻;
- 相较于对照组,组织学评分更佳;
- 炎症标志物(细胞因子、趋化因子)水平下降;
- 粘膜愈合及上皮屏障功能恢复增强。
安全性评估
- 受试动物未出现显著不良反应;
- 纳米颗粒配方耐受性良好;
- 系统性暴露极低,进一步印证了靶向递送的优势。
未来方向与临床转化
该纳米递送系统的成功为后续研究和临床开发打开了多条道路:
扩展肽库
平台技术可用于递送其他治疗性肽或蛋白,拓宽对多种炎症性疾病的治疗选项。
组合疗法
纳米颗粒可装载多种药物,实现针对炎症级联反应的组合治疗。
个性化医疗
通过调整表面功能化或更换载药成分,可为不同患者的疾病特征量身定制治疗方案。
临床试验设计
- I 期:健康志愿者安全性评估;
- II 期:溃疡性结肠炎患者的概念验证;
- III 期:大规模疗效与安全性随机对照试验。
监管考量
- 纳米颗粒配方的表征与标准化;
- 生产工艺的一致性与质量控制;
- 长期安全性监测;
- 与现有标准疗法的比较研究。
对药物递送科学的更广泛影响
此突破不仅意味着一种新的溃疡性结肠炎治疗方案,更展示了先进纳米递送系统变革治疗思路的潜力。
范式转变
从传统的全身给药转向精准靶向治疗,可在降低副作用的同时提升疗效。
技术平台
透明质酸功能化纳米颗粒可作为模板,开发针对以下疾病的治疗方案:
- 克罗恩病;
- 类风湿性关节炎;
- 炎症性皮肤病;
- 其他自身免疫疾病。
经济意义
成功商业化有望:
- 提升治疗效果,降低医疗支出;
- 减少住院及并发症发生率;
- 为患者提供比昂贵生物制剂更可负担的选择。
挑战与注意事项
尽管前景光明,仍需克服若干障碍才能实现临床落地:
- 规模化生产:大批量制造一致性高的纳米颗粒需要先进工艺与严格质量控制;
- 长期安全:需对重复给药的长期影响进行深入评估;
- 患者差异:不同患者的生理、疾病严重程度及基因背景可能影响疗效,需要制定个体化剂量方案;
- 监管路径:纳米药物的复杂性可能需要新颖的评估框架和监管指引。
结论
透明质酸功能化纳米颗粒用于靶向递送 KPV 三肽的研发标志着肽类治疗和药物递送科学的里程碑。通过克服肽的稳定性、生物利用度和定位难题,该创新为治疗炎症性肠病乃至更广泛的炎症性疾病提供了全新思路。
该技术展示了将天然治疗分子与先进递送平台结合的巨大潜力,能够在保持疗效的同时提升安全性。随着临床试验的推进,这一方案有望为溃疡性结肠炎患者乃至其他炎症性疾病患者带来更有效、靶向且成本可承受的治疗选择。
更重要的是,这一突破提供了一套通用平台技术,可能彻底改变我们在全身递送治疗性肽和蛋白质时的策略。随着个性化医疗的持续发展,精准递送系统将在优化治疗效果、最小化副作用方面发挥日益重要的作用。
对全球数以百万计的炎症性肠病患者而言,这不仅是科学的进步,更是通过更有效、靶向治疗提升生活质量的希望之光。实验室的突破正向临床转化迈进,而这项研究奠定的坚实基础将推动未来更多创新疗法的诞生。