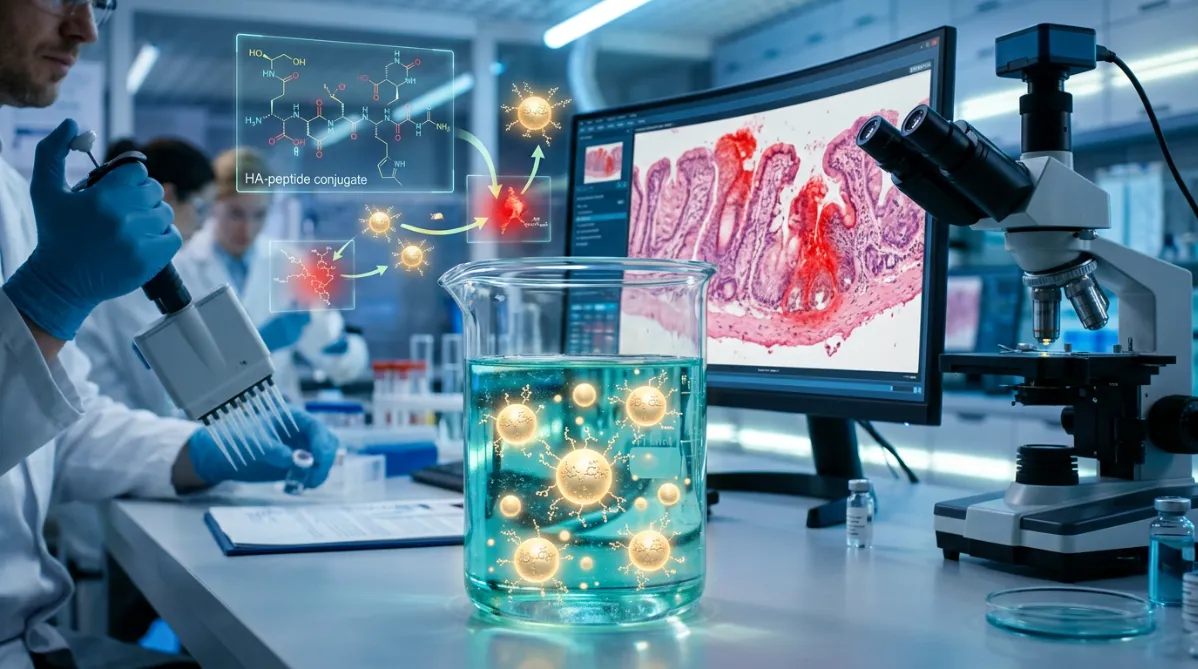
標的型ペプチド送達の突破口
炎症性腸疾患、特に潰瘍性大腸炎の治療を根本から変える可能性のある新しい送達システムが登場した。ジョージア州立大学とサウスウェスト大学の研究チームは、ヒアルロン酸で機能化したナノ粒子を用いて、炎症が起きた腸組織へ治療用ペプチドを正確に届けることに成功した。これにより、世界中の何百万人もの患者に新たな希望がもたらされる可能性がある。
この革新的なシステムは、現代医療が抱える最大の課題の一つである「治療剤を体内の目的部位へ正確に届け、副作用を最小限に抑える」ことに応えるものだ。従来の経口薬は吸収率が低く、消化管内で急速に分解され、全身へ非特異的に分布するため、有効性が低く副作用が出やすい。
KPVトリペプチド:自然由来の抗炎症剤
この突破口の核心は、α‑メラノサイト刺激ホルモン(α‑MSH)由来の自然由来トリペプチド、リシン‑プロリン‑バリン(KPV)である。この小さくて強力な分子は優れた抗炎症作用を示し、炎症性腸疾患の治療に理想的な候補となる。
「KPVはペプチド治療の重要な前進です」と、本研究に直接関わっていない消化器専門医のサラ・ミッチェル博士は語った。「合成薬が大きな副作用を伴うのに対し、この自然由来化合物は体内の抗炎症経路と協調して働きます」
KPVは核因子κB(NF‑κB)経路など主要な炎症シグナル伝達経路を調節し、炎症が起きた腸管でのプロ炎症と抗炎症のバランスを回復させる。しかし、経口投与時の安定性が低く、すぐに分解されてしまうという課題があった。ペプチドは胃の強酸性環境や各種消化酵素により分解されやすく、効果的な経口送達は極めて困難である。
ヒアルロン酸:最適なキャリア
研究チームは、KPVをヒアルロン酸(HA)で機能化したナノ粒子にカプセル化することでこの課題を克服した。ヒアルロン酸はヒトの体内に広く存在する天然ポリマーで、以下の重要な機能を果たす。
標的認識
ヒアルロン酸はCD44受容体に特異的に結合する。CD44は炎症性腸上皮細胞や、炎症性腸疾患に関与する免疫細胞の表面に過剰に発現している。この受容体依存的な標的化により、治療ペイロードが最も必要な部位へ正確に届けられる。
安定性向上
HAコーティングは消化酵素や胃酸からカプセル化されたKPVを保護し、活性成分がそのまま目的部位に届く割合を高める。
バイオアベイラビリティ改善
ナノ粒子化により、従来の遊離ペプチド投与に比べKPVの吸収率とバイオアベイラビリティが向上し、炎症部位での有効濃度が上昇する。
粘膜接着性
ヒアルロン酸は粘膜接着性を有し、腸管の粘液層に結合できる。この接着によりナノ粒子の腸内滞留時間が延長され、ペプチドの持続的放出が可能になる。
ナノ粒子設計:分子レベルの精密さ
有効なナノ粒子送達システムの開発には、分子レベルでの精密な設計が必要である。研究チームは次の重要パラメータを最適化した。
粒子サイズと分布
ナノ粒子は直径約100〜200 nmに設計され、以下の点で最適化されている。
- 粘液バリアを通過できるほど小さい
- 腎臓による迅速なクリアランスを回避できるほど大きい
- エンドサイトーシスによる細胞取り込みに最適
表面電荷
表面電荷は生体膜との相互作用や生体液中での安定性に影響する。HA機能化により、細胞取り込みを促進しつつ安定性を保つ適切な電荷が付与される。
薬物装填効率
研究者は高い装填効率を実現し、各ナノ粒子が治療上有意義な量のKPVを保持できるようにした。この効率は総投与量を抑え、副作用リスクを低減する上で重要である。
放出動態
ナノ粒子はKPVを長時間にわたって制御放出するよう設計されており、標的部位での治療濃度を維持しつつ全身曝露を最小化する。
潰瘍性大腸炎治療への臨床的示唆
潰瘍性大腸炎は米国だけでも約100万人が罹患しており、血便・腹痛・頻繁な排便などの症状を伴う慢性炎症性疾患である。現在の治療法は以下の通りだ。
現行療法
- 5‑アミノサリチル酸(5‑ASAs):第一選択薬として使用されるが、全患者に有効とは限らない
- コルチコステロイド:強力な抗炎症薬だが、長期使用で重大な副作用が生じる
- 免疫抑制剤:免疫系を抑制するが感染リスクが上昇する
- バイオロジクス:標的療法だが高価で、時間とともに効果が減衰することがある
現行アプローチの課題
- 非特異的分布による全身性副作用
- 患者間での効果のばらつき
- 抵抗性や効果喪失の発生
- バイオロジクスの高コスト
- 頻回投与や侵襲的投与経路の必要性
新送達システムの利点
- 標的送達:CD44受容体を介した炎症組織への選択的結合により、正常組織への曝露を最小化し副作用を低減する。
- 有効性向上:バイオアベイラビリティと標的化が改善され、炎症部位での治療濃度が上昇する。
- 投与頻度削減:持続放出特性により投与回数が減少し、患者のコンプライアンスが向上する。
- コスト効果:KPVとHAという天然成分を使用するため、高価なバイオロジクスに比べ治療費が抑えられる可能性がある。
- 安全性向上:治療剤とキャリアが自然由来であるため、耐容性が高いと期待できる。
実験的検証と結果
研究チームは包括的な前臨床試験を実施し、送達システムの有効性を評価した。主な所見は以下の通りである。
試験管内実験
- 炎症細胞上のCD44受容体への特異的結合を確認
- 24〜48時間にわたるKPVの持続放出を実証
- 細胞培養モデルでの抗炎症活性を確認
動物実験
- マウスの潰瘍性大腸炎モデルで大腸炎症が顕著に軽減
- コントロール群に比べ組織学的スコアが改善
- サイトカイン・ケモカインなど炎症マーカーが低下
- 粘膜の治癒と上皮バリア機能の回復が促進
安全性評価
- 投与動物に顕著な副作用は認められなかった
- ナノ粒子製剤は良好な忍容性を示す
- 全身曝露が最小限であることが標的送達を裏付ける
今後の展望と臨床翻訳
このナノ粒子送達システムの成功は、今後の研究と臨床開発に多くの可能性を提供する。
- ペプチドライブラリの拡大:本プラットフォームは他の治療用ペプチドやタンパク質の送達にも応用でき、様々な炎症性疾患の治療選択肢を広げる。
- 組み合わせ療法:複数の治療薬を同時に搭載できるため、炎症カスケードの異なる段階を同時に標的化する併用療法が実現可能。
- 個別化医療:表面機能化や搭載薬剤を変更することで、患者ごとの疾患特性に合わせたカスタマイズが可能になる。
- 臨床試験設計:
- 健康志願者を対象とした第Ⅰ相安全性試験
- 潰瘍性大腸炎患者を対象とした第Ⅱ相概念実証試験
- 大規模第Ⅲ相有効性試験
- 規制上の考慮点:
- ナノ粒子製剤の特性評価
- 製造プロセスの一貫性と品質管理
- 長期安全性の検証
- 既存標準治療との比較評価
医薬品送達科学への広範な影響
このブレークスルーは単なる潰瘍性大腸炎治療に留まらず、精密なナノ粒子送達システムが治療介入の在り方を変える可能性を示す。
パラダイムシフト
全身投与から標的型療法への転換は、副作用を低減しつつ治療効果を最大化する新たな潮流を示す。
技術プラットフォーム
HA機能化ナノ粒子は以下の疾患に対する治療開発の雛形となり得る。
- クローン病
- 関節リウマチ
- 炎症性皮膚疾患
- その他自己免疫疾患
経済的インパクト
本技術の実用化は、治療効果の向上による医療費削減、入院や合併症の減少、そして高価なバイオロジクスへの代替手段提供を通じて医療経済に貢献する。
課題と留意点
有望な結果が得られた一方で、臨床応用にはいくつかの課題が残る。
製造スケーラビリティ
商業規模での一貫した品質のナノ粒子生産には高度な製造プロセスと品質管理が不可欠である。
長期安全性
初期の安全性データは有望だが、繰り返し投与による長期的影響は詳細に評価する必要がある。
患者間変動
個々の生理学的状態、疾患重症度、遺伝的背景が治療反応に影響を与える可能性があるため、個別投与戦略が求められる。
規制承認
ナノ粒子製剤の複雑さは規制上の新たな評価枠組みを必要とし、承認プロセスが従来と異なる課題を呈する。
結論
KPVトリペプチドを標的送達するためのヒアルロン酸機能化ナノ粒子の開発は、ペプチド治療と薬剤送達科学の両面で重要なマイルストーンである。ペプチドの安定性、バイオアベイラビリティ、標的送達という根本的課題を克服したことで、炎症性腸疾患や他の炎症性疾患の治療に新たな可能性が開かれた。
自然由来の治療化合物と高度な送達技術の組み合わせは、より効果的で安全な治療法を創出する力を示す。本技術が臨床試験へと移行すれば、潰瘍性大腸炎はもちろん、他の炎症性疾患を抱える患者にも新たな希望をもたらすだろう。
このブレークスルーは単一疾患にとどまらず、全身のペプチド・タンパク質送達プラットフォームとして医療を根本的に変える可能性を秘めている。個別化医療が進展する中、標的型送達システムは治療効果の最適化と副作用の最小化に不可欠な要素となるだろう。
炎症性腸疾患に苦しむ数百万の患者にとって、この技術は単なる科学的進歩ではなく、より良い生活実現への大きな一歩となる。研究室からベッドサイドへの道のりはまだ続くが、今回の研究が築いた基盤は将来の治療イノベーションの強固な土台となる。